干细胞疗法工艺开发的关键点 从实验室到临床的转化之路
干细胞疗法作为再生医学领域的前沿技术,在治疗退行性疾病、组织损伤修复以及免疫调节等方面展现出巨大潜力。要将这一前沿技术成功转化为安全、有效、稳定的临床产品,其工艺开发是关键且复杂的环节。本文将围绕干细胞疗法工艺开发的核心技术要点进行梳理,为相关研究与产业化提供参考。
1. 细胞来源与质量标准的建立
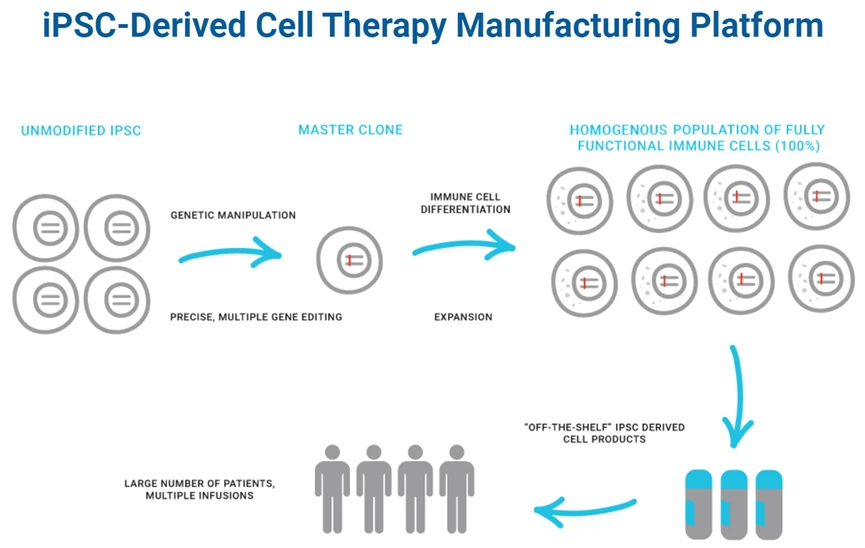
干细胞疗法的首要关键是确定可靠且合规的细胞来源。无论是胚胎干细胞(ESCs)、诱导多能干细胞(iPSCs)还是成体干细胞(如间充质干细胞MSCs),其获取、筛选和鉴定都必须遵循严格的标准。建立全面的细胞身份鉴定(如表面标志物、基因型)、纯度(无其他细胞污染)和安全性(如无菌、无支原体、无特定病原体)的质量控制体系是工艺开发的基石。特别是对于iPSCs,其重编程过程的效率和安全性、以及可能存在的基因组不稳定性,都需要在工艺早期进行充分评估和控制。
2. 规模化扩增与培养工艺优化
从实验室的少量培养到满足临床需求的大规模生产,是干细胞疗法工艺开发的核心挑战。这涉及到:
- 培养体系:开发成分明确、无异源(如无动物血清)的培养体系,以确保产品的安全性和一致性。
- 生物反应器应用:从传统的培养皿转向可监控、可放大的生物反应器(如搅拌式、固定床式反应器),以实现细胞的高密度、均一化生长,并严格控制温度、pH、溶氧等关键参数。
- 细胞传代与衰老控制:优化传代方法,防止细胞在扩增过程中发生表型改变、功能丧失或衰老。
3. 分化与功能诱导的精准控制
对于需要特定功能细胞(如心肌细胞、神经元、胰岛β细胞)的治疗,如何高效、定向地将干细胞诱导分化为目标细胞,并确保其功能成熟和稳定,是工艺的难点。这需要:
- 开发化学成分明确、时序精确的分化方案。
- 建立严格的质量控制点,对分化过程中的关键标志物进行实时监测,确保分化效率和细胞纯度。
- 有效去除未分化细胞,以防止畸胎瘤等安全风险。
4. 下游处理与制剂开发
细胞培养完成后,如何收获、洗涤、浓缩、配制和保存细胞,直接影响最终产品的活性和稳定性。
- 收获与分离技术:采用温和、高效的细胞解离方法(如酶解或物理方法),最大限度保持细胞活性和功能。
- 配方与冻存:开发适合长期保存的细胞冻存液配方,优化冻存(降温速率)和复苏流程,确保细胞复苏后保持高活率和治疗功能。
- 制剂与灌装:在符合GMP(药品生产质量管理规范)的条件下,将细胞产品灌装到最终容器中,并确保在储存和运输过程中的稳定性。
5. 全过程质量控制与放行检验
贯穿整个工艺开发,必须建立一个从起始物料到终产品的全链条、多维度的质量控制体系。这包括:
- 过程分析技术(PAT):在线监测关键工艺参数和细胞质量属性。
- 放行检验:对终产品进行强制性检验,如细胞活率、纯度、效力(功能学检测)、无菌、内毒素等,确保每一批次产品都符合预设的安全与有效性标准。
- 稳定性研究:评估产品在拟定储存条件下的有效期。
6. 符合法规的GMP生产体系
干细胞疗法作为先进的治疗用医疗产品(ATMP),其生产必须在符合GMP要求的洁净环境下进行。这包括厂房设施、设备验证、人员培训、文件记录(确保全程可追溯)、以及严格的质量管理体系的建立。工艺开发阶段就必须与监管要求紧密结合,确保数据完整可靠,为临床试验申请(IND)和上市申请(BLA/MAA)奠定坚实基础。
###
干细胞疗法工艺开发是一个多学科交叉、技术密集的系统工程。它不仅仅是实验室技术的放大,更是将生物学、工程学、质量控制与法规科学深度融合的过程。成功的关键在于早期规划、全过程控制、以及对产品质量和安全性的不懈追求。随着技术的不断成熟和标准化,稳定、可放大的生产工艺必将推动更多安全有效的干细胞疗法惠及广大患者。
如若转载,请注明出处:http://www.yinmeisaier.com/product/4.html
更新时间:2026-03-07 07:10:35